3 - mémoire et apprentissage
I - Stockage des informations au niveau des synapses
- Structures et fonctions
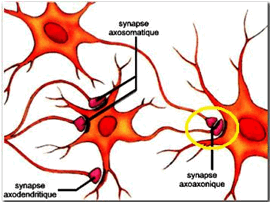
On distingue trois types structuraux :
- les synapses axoaxoniques liées à un axone
- les synapses axodendritiques liées à une dendrite
- les synapses axosomatiques liées à un corps cellulaire
On compte deux types fonctionnels :
- les synapses électriques dans lesquelles le potentiel d’action excite l’élément post-synaptique (inversion de la polarité de la membrane) afin de transmettre le signal électrique
- les synapses chimiques dans lesquelles le potentiel d’action provoque une libération de substance chimique
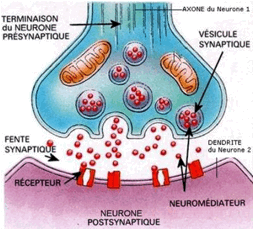
- Les messagers cérébraux ou neuromédiateurs
A nouveau, on distingue deux sortes de neuromédiateurs : les neurotransmetteurs responsables de la neurotransmission et les neuromodulateurs, responsables de la neuromodulation. Il s’agit donc de deux types de communications chimiques.
Lorsque le neurotransmetteur est libéré, il active un récepteur canal (protéine de la membrane) qui laisse passer les ions et informe l’élément post-synaptique qui engendre une réponse cellulaire très rapide.
Concernant les neuromédiateurs (voir schéma au dessus), leur récepteur est constitué de trois unités sous-protéïques dont l’une correspond au site de fixation du neuromodulateur, la seconde étant une unité de modulation et la dernière une unité catalytique (site d’action d’une enzyme). Il peut s’agir de l’adrénaline, du GABA ou encore de la sérotonine. Leur réponse est toutefois plus lente que celle des neurotransmetteurs.
Le critère de répartition entre les systèmes neuroniques dépend de la diffusion de la population neuronale : s’ils sont répartis de manière diffuse dans le cerveau, la transmission se fera par neuromodulation, s’ils sont localisés à un ou deux endroits précis, c’est la neurotransmission qui entrera en jeu. On dit donc que les systèmes neuroniques sont contexte-dépendants, cela signifie que la substance chimique mobilisée dépendra de la zone du cerveau.
II - Les modifications synaptiques
- Les modifications neurochimiques
Lors d’un apprentissage, un axone A transmet l’information à un axone B qui augmente alors sa concentration en neuromédiateurs afin de conduire l’information à un neurone C. Cependant, si la quantité de récepteurs du neurone C n’augmente pas en même temps que la quantité de neuromédiateurs, alors l’information est perdue. Cette augmentation de récepteurs post-synaptique est appelée hypersensibilité.
Par ailleurs, pour tout nouvel apprentissage, les structures des synapses se modifient, créant ainsi de nouvelles ramifications synaptiques. De même, un axone B, qui possède des liens avec deux axones A et C, pourra être stimulé davantage par un des deux liens. Dans ce cas, le lien stimulé sera renforcé alors que le lien non stimulé, dégénèrera.
Pour provoquer des changements neurochimiques et structuraux, plusieurs conditions sont toutefois requises : l’élément pré-synaptique doit souvent stimuler l’élément post-synaptique de façon à engendrer un influx nerveux fréquent. De plus, deux éléments pré-synaptiques ayant tendance à activer le même élément post-synaptique auront tendance à se connecter entre eux, c'est-à-dire à former une synapse.
On appelle l’hypothèse de double trace, le postulat selon lequel un individu soumis à l’apprentissage d’une tâche développera une activité neuronale, laquelle, si elle est suffisamment forte, entraînera des modifications structurales et neurochimiques qui deviendront permanentes, susceptibles d’intervenir dans la mémoire à long terme.
- L’expérience de Held et Hein
Ils placèrent deux chatons dans un cylindre peint de bandes noires et blanches. Les deux chatons sont déposés sur des nacelles, mais seul le chaton 1 peut agir pour faire tourner la nacelle du chaton 2. Dans une seconde phase, les deux chatons sont placés sur un parcours d’obstacle, représentant la première épreuve visuo-motrice pour les deux animaux. Le premier chaton y parvient, alors que le second échoue.
Cette expérience détermine la notion de période sensible : les deux chatons ont reçu les mêmes stimulations visuelles mais seul le premier chaton a également reçu des stimulations motrice. Après un certain temps, le chaton 2 s’avère incapable de témoigner d’une capacité conjuguant vision et motricité. Cependant, si le chaton 2 est stimulé suffisamment tôt, il parviendra à acquérir cet apprentissage, d’où la notion de période sensible.
Remarque : dans les crèches ou écoles maternelles, l’environnement est coloré et riche, de façon à stimuler l’enfant, développer les productions de synapses et intensifier l’adaptation.
- Expérience d’enrichissement environnemental
Dans une première condition standard, on place trois rats dans une cage, dans la condition 2, un rat est placé seul dans une cage, et dans une troisième condition, on place 6 rats dans une cage contenant divers jeux tels une roue etc…
Après un certain temps, les chercheurs analysèrent leurs modifications synaptiques : dans la troisième condition présentant un environnement riche, une augmentation du poids du cortex a été observée ainsi qu’une croissance de son épaisseur (chez l’Homme, ce processus est appelé lamination). De même, ont évolué le nombre et la surface des synapses, l’arborisation denditrique (davantage d’informations passent et arrivent), et l’activité de l’enzyme acetylcholinestérase permettant la synthèse de l’Ach.
Des modifications ont également été observées dans le cervelet, elles seraient corrélées à un apprentissage moteur de l’équilibre.
III - Implication du cervelet dans la mémoire : la dépression à long terme
-
Anatomie du cervelet
- Les cellules de Purkinje
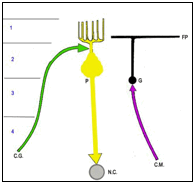 |
1 : couche superficielle (moléculaire)
P : Cellule de Purkinje |
Les cellules de Purkinje forment la première couche cellulaire et possèdent une arborisation dendritique très dense qui se distribue au dessus, dans la couche moléculaire superficielle du cervelet. Leurs axones innervent les noyaux profonds qui innervent eux-mêmes les autres structures du cerveaux.
Dans le cas de l’afférence nerveuse, les cellules de Purkinje reçoivent l’influx nerveux grâce aux fibres grimpantes provenant de l’olive inférieure, elle-même située au niveau du bulbe rachidien.
- Les fibres parallèles
Les fibres parallèles proviennent des cellules localisées dans le point et envoient leurs axones dans la couche granulaire : il s’agit des fibres moussues représentant environ la moitié des neurones du cervelet. Elles innervent elles-mêmes les dendrites des cellules de Purkinje et possèdent un axone en forme de T.
- Action des cellules de Purkinje et des fibres parallèles
Le neuromédiateur utilisé par les cellules de Purkinje et les fibres parallèles est le GABA (acide gama-amino butyrique). Il s’agit d’un acide aminé inhibiteur : les cellules de Purkinje exercent donc une action inhibitrice sur les noyaux profonds du cervelet.
A l’inverse, les fibres parallèles exercent une action excitatrice sur les cellules de Purkinje via le glutamate, un acide aminé excitateur.
- Le cervelet comme support d’un apprentissage moteur : l’hypothèse de Marr-Albus
Son hypothèse affirme que la double innervation des cellules de Purkinje par les fibres grimpantes et les fibres parallèles constitue le support neurochimique de l’apprentissage moteur.
Dans un premier temps, la fibre grimpante transporte les informations provenant d’un mouvement défectueux tel qu’une perte d’équilibre. Pour rattraper ce mouvement, les fibres parallèles s’activeraient : il existerait donc une plasticité de la synapse reliant les cellules de Purkinje et les fibres parallèles.
- La dépression à long terme
L’hypothèse de Marr-Albus fut validée par les travaux conduits par Ito. Celui-ci provoqua une stimulation des fibres parallèles de la même façon que l’aurait fait un mouvement défectueux, et créa ainsi un potentiel post-synaptique excitateur de forte amplitude.
Puis il effectua une stimulation commune des fibres parallèles et des fibres grimpantes avant de provoquer à nouveau une simple stimulation des fibres parallèles. Il constata alors que l’amplitude du potentiel post-synaptique excitateur était plus faible que lors de la première stimulation et que cette diminution se prolongeait durant une heure : il s’agit de la dépression à long terme, phénomène qui représenterait le support neurochimique de l’apprentissage moteur.
- Les mécanismes moléculaires de la dépression à long terme
Lorsque les fibres grimpantes activent les cellules de Purkinje, le potentiel post-synaptique excitateur entraîne la dépolarisation de la membrane plasmique, l’échange d’ions de sodium (Na+) et libère du potassium de la membrane :
- les canaux à ions sodium s’ouvrent
- les canaux à calcium (Ca²+) s’ouvrent sous l’effet de l’amplitude du potentiel post-synaptique excitateur
- les fibres parallèles libèrent du glutamate, activant le canal Ampa (spécifique du glutamate) et permettant au sodium d’entrer à l’intérieur de la cellule.
- l’activation du récepteur du canal ionotropique Ampa à l’intérieur de la cellule active le phospholipase C, une enzyme, qui active elle-même un second messager, stimulant la kinase C, une protéine ayant pour fonction de transformer les protéines
La mémoire est donc associée aux modifications des récepteurs Ampa ainsi qu’à la diminution des effets excitateurs. L’apprentissage laisse une trace moléculaire : l’entrée de sodium et de calcium et d’autres molécules : on parle de cascade moléculaire.
Si la dépression à long terme joue un rôle dans l’apprentissage moteur, on peut dire que l’apprentissage et la mémoire résultent sans doute de modification de la transmission synaptique, celles-ci étant déclenchée par la conversion de l’activité nerveuse en second messager intracellulaire. Les souvenirs se forment ensuite à partir de la transformation de protéines pré-existantes.
IV - Les systèmes neuromodulateurs diffus
- Généralités
La neuromodulation s’oppose à la neurotransmission dans la mesure où elle complète et module les actions rapides de la neurotransmission. Elle se charge donc des réponses lentes, des régulations et agit de façon diffuse.
Il existe plusieurs systèmes neuromodulateurs diffus :
- le système noradrénergique (noradrénaline NA)
- le système sérotoninergique (sérotonine 5HT)
- le système dopaminergique (dopamine DA)
- le système cholinergique (acétylcholine Ach)
-
L’organisation anatomo-fonctionnelle des systèmes neuromodulateurs diffus
- Le système noradrénergique
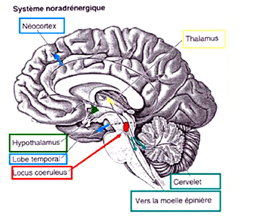
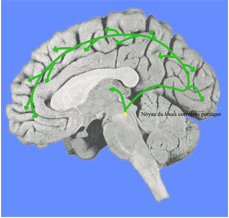
Ce système se distribue dans toutes les aires corticales. Les neurones noradrénergiques sont actifs dés que se présente une nouveauté dans l’environnement et sont donc considérés comme augmentant la sensibilité du cerveau à l’environnement.
Ils sont également impliqués dans les cycles de veille et de sommeil, les apprentissages et la mémoire, la régulation du métabolisme cérébral, les troubles de l’humeur, de l’anxiété et du stress ainsi que dans les actes volontaires.
- Les systèmes sérotoninergiques
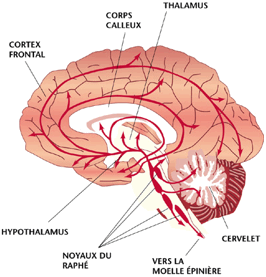
Leurs corps cellulaires sont aussi localisés dans le tronc cérébral, plus précisément dans le noyau du Raphé. Dans le bulbe rachidien, les corps cellulaires postérieurs projettent la sérotonine vers la moelle épinière où ils contrecarrent la sensation de douleur provenant de la périphérie. Les corps cellulaires antérieurs sont, quant à eux, situés dans le pont, le mésencéphale et projettent vers toutes les régions cérébrales.
Les neurones sérotoninergiques sont impliqués dans presque toutes les fonctions mentales : la faim, la sexualité, les émotions et les troubles de l’humeur, l’anxiété et le stress ou encore la coordination motrice. Leurs actions dépendent des structures innervées et du type de récepteurs à la sérotonine utilisés (il en existe 14). Toutefois, un sous-récepteur peut également être impliqué dans plusieurs fonctions mentales.
Les régions les plus richement innervées par la sérotonine sont le globus pallidus qui appartient au ganglion de la base, la substance noire et l’hippocampe.
- Les systèmes dopaminergiques
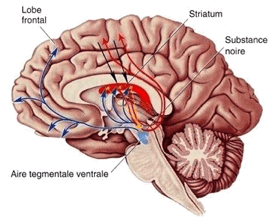
Leurs corps cellulaires sont localisés dans le mésencéphale et possèdent deux noyaux :
- la partie contact de la substance noire constituée par les corps cellulaires exprimant la dopamine : ils projettent sur le noyau caudé et le putamen et représentent la voie par excellence des comportements moteurs
- l’aire tegmentale ventrale qui projettent sur le noyau accumbens (partie ventrale par rapport au caudé-putamen. Il s’agit de la voix du plaisir qui est activée après une récompense ou encore une administration de cocaïne ou d’amphétamine qui augmente la libération de dopamine (on pense que le mécanisme serait le même chez les schizophrènes).
Ils sont également impliqués dans le cycle veille/sommeil, les processus motivationnels et attentionnels ainsi que dans la planification des mouvements.
- Les systèmes cholinergiques
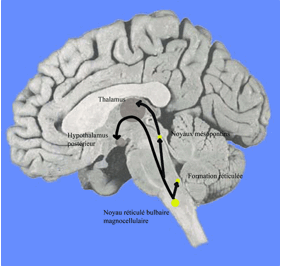
Ces neurones expriment l’acétylcholine, leurs corps cellulaires sont regroupés dans le noyau basal de Meynert (position ventrale par rapport au globus pallidus) ainsi que dans les noyaux du septum (entre les ventricules latéraux). Ils projettent vers le corps cérébral dans le système pontmésencéphalotegmental, c'est-à-dire vers le thalamus dorsal.
Ils sont impliqués dans la régulation des informations sensorielles, c'est-à-dire la sensibilité extéroceptive, en complément de deux autres neuromodulateurs (la sérotonine et la noradrénaline). Dans le cas de la maladie d’Alzheimer, on observe une dégénérescence des neurones du noyau basal de Meynert, mais il peut s’agir d’une conséquence et non d’une cause.
- Un autre système neuromodulateur diffus : les neuropeptides ou peptidergiques
Les peptides furent découverts en 1974 ‘grâce’ aux injections de morphine. La diminution de la douleur impliquait en effet qu’il en existe des récepteurs internes, alors même qu’il s’agissait de substances endogènes (extérieur au corps) : ce sont les peptides.
L’enképhaline, l’endorphine ou encore la dynorphine (par exemple) sont synthétisés dans les corps cellulaires de l’hypothalamus, du thalamus, du globus pallidus ainsi que dans des structures appartenant au système limbique.
Le rôle des peptides est d’agir contre la douleur telle des analgésiques mais également d’intervenir dans les mécanismes du plaisir en produisant un sentiment d’euphorie. Par ailleurs, les dépressions sont dues en partie à des évolutions du taux d’enképhaline.
On distingue également le peptide substance P. contenue dans la substance noire et dans la moelle épinière et véhiculant l’information de douleur et donc inhibée par l’enképhaline.
-
Exemples de relations entre système neuromodulateur diffus et fonctions mentales
- L’émotion
Le centre émotionnel du cerveau est le système limbique qui traite les émotions liées à la survie et au plaisir. L’hippocampe appartenant au système limbique, cela explique que les fortes émotions soient aussi les plus facilement mémorisées, tout comme les bulbes olfactifs qui sont le seul sens dont les fibres nerveuses sont interconnectées au système limbique : c’est ainsi que nous retenons mieux les odeurs.
- L’agressivité
L’agressivité est essentiellement liée à des évolutions du taux de sérotonine. Par exemple, lorsque l’on observe des rats en cage, ceux qui sont agressifs présentent une altération de la synthèse de sérotonine. Si on leur injecte du PCPA (parachlorophénylalanine) qui bloque la synthèse de sérotonine, le comportement agressif s’intensifie.
On a également pu observer des modifications de comportements chez des souris transgéniques pour lesquels avait été supprimé un gène codant pour un récepteur de la sérotonine : de ce fait, les souris étaient plus agressives mais également plus anxieuses : on comprend donc que pour une même fonction mentale, il existe au moins deux systèmes neuronaux impliqués.
- Dopamine et circuits neuronaux liés au plaisir
Dans une expérience conduite par Olds et Milner, une électrode avait été implantée dans une structure nerveuse d’un rat. S’il se déplaçait du haut vers la gauche, il recevait une stimulation électrique, le fait qu’il y retourne a prouvé qu’il appréciait la stimulation. Ils utilisèrent ensuite le même mécanisme mais en envoyant la stimulation au rat après qu’il ait appuyé sur une manette : c’est ce qu’on appelle l’autostimulation.
Lors de ces stimulations, ils observèrent une activation de l’aire tegmentale ventrale. Celle-ci contient les neurones à dopamine. Si l’on injecte de l’amphétamine au rat, qui a pour effet d’augmenter le taux de dopamine, les comportements d’autostimulations augmentent en fréquence. A l’inverse, si l’on utilise des antagonistes à la dopamine, les comportements d’autostimulations régressent.